記者蔣季容/台北報導

▲全台首例「欣智樂」23日施打。(圖/亞東醫院提供)
台灣失智人口突破35萬人,其中7成為阿茲海默症患者。隨著失智症趨勢日益高齡化與年輕化,延緩退化、維持生活品質成為當前醫療重要課題。衛福部近期核准2款早期阿茲海默症創新針劑「樂意保(Leqembi)」與「欣智樂(Kisunla)」,正式為台灣失智治療開啟新里程。亞東醫院於6月23日完成首例新藥「欣智樂」注射,接受治療者為83歲女性,診斷為早期阿茲海默症。她經過影像檢查、基因評估及專業團隊審查後,成為全國第一位接受此創新療法的患者。
亞東醫院神經醫學部失智中心主任甄瑞興表示,該名患者雖年事已高,但日常生活功能仍良好,能獨自搭乘大眾運輸、處理家務,甚至在家協助照顧患有失智症的配偶。她因發現自己出現健忘、重複提問等異狀,加上家中已有失智案例,主動前來就醫檢查。
經初步評估,患者認知功能障礙檢查(CASI)為92分(滿分100分)、簡易心智量表(MMSE)為29分(滿分30分),顯示為輕度認知障礙。後續經核磁共振、正子斷層掃描(PET)與基因篩檢,確認其腦中已有類澱粉蛋白沉積,且符合新藥的適應症條件。甄瑞興指出,這正是藥物介入的黃金時機。新藥的目的不是逆轉記憶,而是延緩退化,延長患者維持日常生活能力的時間,守住清醒且有尊嚴的生活品質。

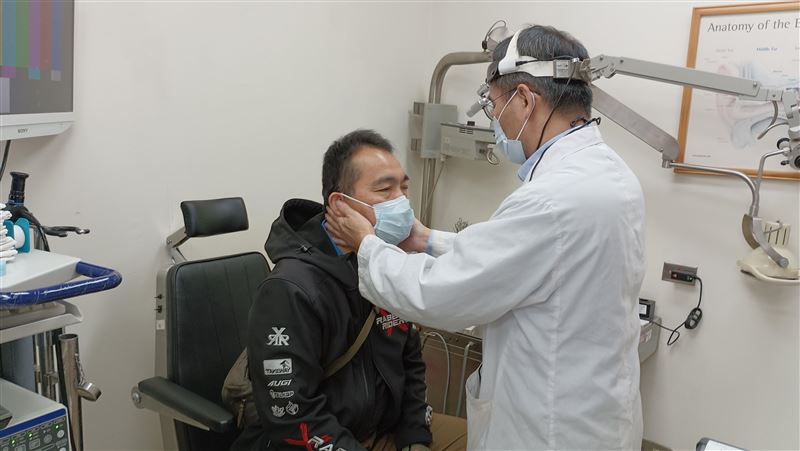
▲83歲婦(左)施打欣智樂。(圖/記者蔣季容攝影)
這次衛福部核准的2款新藥,皆屬為單株抗體類藥物,透過清除腦中致病的類澱粉蛋白,從源頭延緩神經退化,是台灣20年來首次引進針對阿茲海默症病因的治療新藥:
樂意保(Leqembi):由日本衛采與美國百健共同研發,每兩週施打一針,1年半後可延長為每月施打一次。類澱粉累積較低的早期患者可減緩至51%。約延緩3年進入中重度的時間。
欣智樂(Kisunla):由美國禮來開發,每月施打一針,研究指出約66%患者在1年後可完全清除類澱粉蛋白;其餘則需約1.5年。部分患者在清除後可暫停施打,但仍需定期追蹤。有助降低50%進展到中度失智風險,或延緩病程約4-5年。
患者女兒表示,雖然新療法的治療費用不低,但考量母親目前仍能獨立生活,決定積極嘗試新藥。她也分享,媽媽每天都會自己安排行程,完成家務、照顧爸爸,這樣的生活對她很重要,「雖然我們知道這不是神藥,但只要能讓她維持現在的狀態久一點,對我們全家來說就是值得的」。這份期待也反映許多家庭對抗失智的心聲,不求奇蹟,只盼多保留一些日常與親情的連結。

▲雖然新藥費用不低,但只要能讓患者維持現在的狀態久一點,對家屬來說就是值得的。(圖/記者蔣季容攝影)
2款藥物皆為靜脈注射,且須於醫院施打;治療前完成澱粉樣蛋白正子攝影(PET)、腦部影像檢查(MRI)與APOE基因檢測等評估。臨床數據顯示,極少數患者可能出現腦水腫或點狀出血,須搭配影像監測,以確保療程安全。
1、1年內曾有中風或癲癇發作病史
2、同時攜帶APOE(ε4/ε4)基因者
3、正服用抗凝血劑者皆屬高風險族群
台灣目前推估約有13萬名患者符合「早期阿茲海默症+類澱粉蛋白陽性」的用藥條件,但因治療費用約每年新台幣100至150萬元,實際可施打人數仍受限。
目前亞東醫院已有10多位早期失智患者完成完整篩檢,其中6、7位符合條件,正與醫師討論是否啟動療程。甄瑞興補充,新藥不是萬靈丹,而是醫療進展的一步,希望能讓病人與家屬知道,有效治療是一段路,還需搭配生活照護、心理支持與長期追蹤,才能真正發揮意義。